
随着人们生活水平的提高,化妆品逐步进(jìn)入了我们的生活(huó),日常(cháng)生活(huó)中我们人人都会与化妆品接触。由于我们的使用频率较高,所以化妆品的质量好坏会影响我们的身体健康,我们需要重(chóng)视。化妆品检测主要是(shì)关注重金属、微生物、抗生素、激素、毒理、抗生素、标(biāo)准禁止添加项目等。
范围:
清洁(jié)类:牙膏、洗面(miàn)奶(膏)、洗发液(膏)、香皂、足
浴盐/沐浴盐、沐浴剂等
护肤类:润肤乳液、润肤(fū)膏霜等
滋养类(lèi):化妆水、面膜、护发素、发乳、发油等
美容类(lèi):化妆粉块、唇膏、香水/古(gǔ)龙水、香(xiāng)粉/爽(shuǎng)身粉/痱子粉、定(dìng)型发胶、发用摩丝(sī)、染发(fā)剂花露水、指甲油等
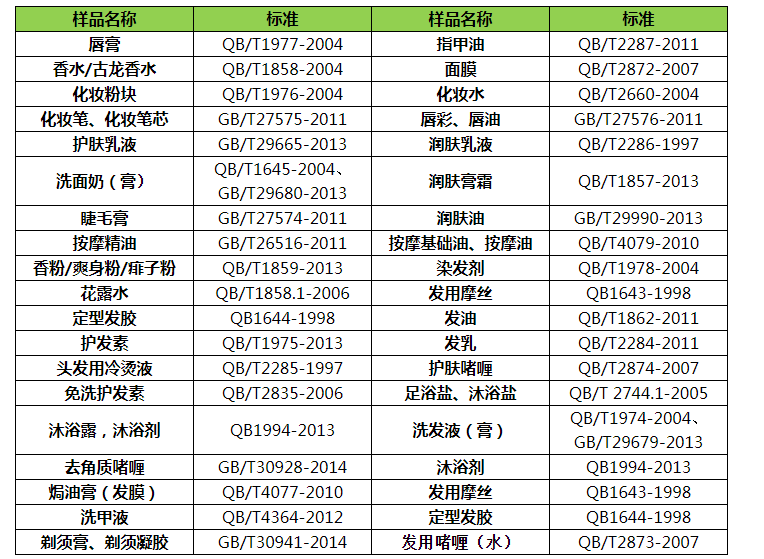
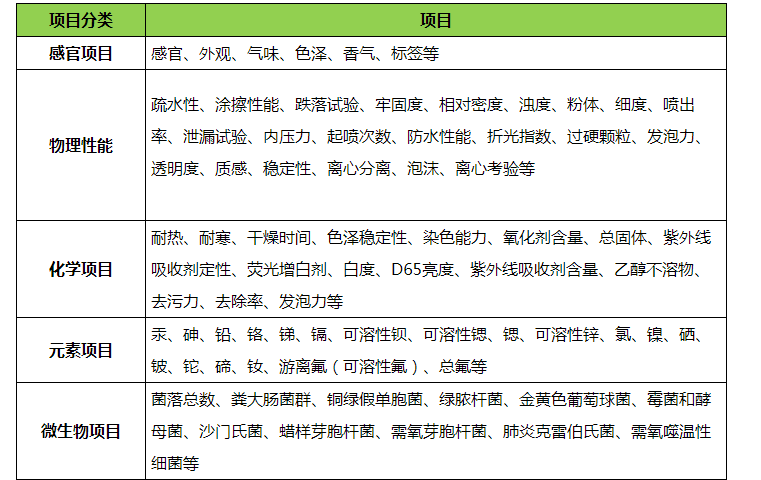

化妆品非特备(bèi)案
特殊(shū)用途化(huà)妆品分别是:育发(fā)、染发、烫发、脱毛、美乳、健美、除臭、祛斑(bān)和防晒9类化妆品,除此之外的化妆(zhuāng)品叫做非特殊用途化妆品,也(yě)就是(shì)普通化妆品(pǐn)。
一、凡在中华人民共和国境内生产(chǎn)的非(fēi)特殊用途化妆(zhuāng)品,生产企业应按本规定(dìng)要求进行产品信息备(bèi)案(àn)。
二、生产企业应当在产品上市销(xiāo)售前,将产(chǎn)品配方(fāng)(不包括含量,限用物质除外)及销售包装(含产品标签、产品说明书)的信息按要求通过统一的网络平台报送至所在行政区域内的省级食品药品监管部门。产品安全性评估资料、产品生产工艺简述、产品生产设备清单、产品技术要求及产品检验报告等资料由生产(chǎn)企业妥善(shàn)保(bǎo)存备查。
三、委(wěi)托生产的产品,委(wěi)托双方(fāng)应分别向所在行政区域内的省级食品药(yào)品监督管理部门报送备案信息。仅供出口的,由实际生产企业向所在(zài)行政区域内的省级食品(pǐn)药品(pǐn)监督管理部门报送备案信(xìn)息(xī)。
四、省级食品药品监(jiān)督管理部门(mén)收到(dào)企业的备案信息后,应当在5个工作(zuò)日内(nèi)完成对备案资料(liào)完整性(xìng)的核查。符合要求的,通过国家食品药品监管(guǎn)总局(jú)政(zhèng)务网公布产品备案信息,供公众(zhòng)查询。
五、对于不属于备案产品范围的、备案资(zī)料不齐全或备案资料不符(fú)合规定形式的,省级食品药品监督管理部门应在5个工(gōng)作日内告知企(qǐ)业(yè)并说明理由。存在明显违法情形的,应当责令立即改正,不得上市销售。
六、省级食品药品监督部门应当在(zài)备案(àn)后三个月内(nèi)组织开展对备案产(chǎn)品的实质审查,发现不(bú)符合国家相关规定的,应当依法予以查处。
七、已经备案的产品,拟变更(gèng)原备(bèi)案事项的,应在变更前将相关变更信(xìn)息报送备案。涉及备案管理部门改变的(de),应主动申请注销原备案信息后,直接申请重新备案。
八、已获备案的产品(pǐn),自备案之日起每满4年(nián)应重新按本规定要(yào)求提交产品备案信息。
九、产品配方(fāng)信息的报送应符合以下要求:
1.全部原料应详细列(liè)明标准中(zhōng)文名称、原料序号、限用物质含量、使用目的等内容。
2.复配原料应以复配形式填报,应标明各(gè)组分的标准中文名称。香精不须列明具体香(xiāng)料组分的种类和含量。
3.原料(含复(fù)配原料中的各组分)应按《国际化妆品原料标准中文名称目录》使用标准中文名称,无国际化妆品原料名称(INCI)或未(wèi)列入《国际化妆品原料标准中(zhōng)文名称目录》的(de),应使用《中国药典》中的名称或化(huà)学名称或植物拉(lā)丁学名,不得(dé)使用商品名或俗名(míng),但复配原料除外。
4.着色剂应提(tí)供《化妆品卫生规范》中载明的着色剂索引号(简称CI号),无CI号的除外。
5.凡在产品配方中使用来源于石油、煤焦油的碳氢化合物的(单一组分的(de)除外),应标明相关原料(liào)的化学文摘索引号(简称CAS号)。
6.使用动物脏器(qì)组织及血液制品提取物(wù)的原料,应当收集该原料的来源、质量规格和原料生产国允许使用的证明等资料(liào)存(cún)档备查。
7.使用《化妆品卫生规范(fàn)》对限用物质有规格要求的原料,应当收集该原料(liào)生产商出具的原料质(zhì)量规(guī)格证明存档备查。
8.宣称为儿童或婴儿使用的(de)产品,配方设计原则(含配方整体分析报告(gào))、原料的选(xuǎn)择原则和要求、生产(chǎn)工艺、质量控制等内容应当按照《儿(ér)童化妆品(pǐn)申报与(yǔ)审评指南(nán)》(国食药监保化[2012]291号)的要(yào)求编制,相关资料应当存档(dàng)备查。
9、产品技术要求的编制参照《关于印发化妆品产品技术要求规范的通知》(国食药监(jiān)许[2010]454号(hào))要求执行;检验(yàn)要求参照《关于印发(fā)化妆品行政许(xǔ)可检(jiǎn)验管理(lǐ)办法的通知》(国食药(yào)监许[2010]82号)执行,其中企业参照(zhào)《关于印发化妆品中可能存在的安全性风险物质风(fēng)险评估指南的通知》(国食药监(jiān)许[2010]339号)要求(qiú)进行风险评估并确认产品安全性的,可(kě)免做(zuò)毒理相关检测。
浙江和诺检测(cè)技术有限公司可以提供样品送检服务,进行非特备案的咨询和指导(dǎo)。
欧盟CPSR(化妆品安全报告)
CPSR(化妆品安全报告)是产品进入欧盟市场的通行证,欧盟化妆品新法规Regulation(EC)1223/2009已于2013年7月11日正式实施,相比于之前的化妆品指令Directive 76/768 EEC,对化妆(zhuāng)品的安(ān)全性提出了更加严格的要求(qiú),其中明确规定了产品必须完成化妆品安全报告(Cosmetic Product Safety Report,CPSR)后方能够在欧盟经济区上市销售。
根据(jù)新法规,欧(ōu)洲化妆(zhuāng)品协会(原(yuán)Colipa)和欧盟委员会共同制定了(le)化妆品安全报告指南(nán),详细解(jiě)读和列出了法规(guī)中关于CPSR的要求(qiú)。该(gāi)指南文件于(yú)2013年11月 25日由欧盟委员(yuán)会作为委员会决议(Commission Decision)发布(bù),欧盟委员会决议具有法律效率,因此企业必须遵(zūn)从该决议。目前进行的(de)毒(dú)理学风(fēng)险评估(Toxicological Risk Assessment,TRA)以及类似的简单升级(jí)版本已经不能够满足CPSR以及该指南的(de)要求。指南更加细化了新法规关于CPSR的要(yào)求。增加的重(chóng)要细则如下:
1. 产品配方中的各(gè)组分需(xū)提供准确的含量,若无法提(tí)供定量信息则按照高剂量计算。复杂成分如提取物或(huò)生物制品等需提(tí)供纯度标准及测(cè)试方法。
2. 产品中使用的原材料供应(yīng)商须在报告中指出,香料和香精必须提供生产商和产品代(dài)码信息。
3. 化妆品包装材料需要满足食品接触材料(Food Contact Material)的标准并保证其稳定性。特(tè)别对于一些对光和空(kōng)气敏感的产品,其正确的贮存方法需要在标(biāo)签上得以体现。
4. 产(chǎn)品需要提供(gòng)稳定性(Stability)报告,其(qí)中(zhōng)包(bāo)括稳定性测定方法,防腐剂挑战试验报告,产品有效期以及开盖使用日期(Period-after-opening)。
5. 化妆品微生物方面的要求进一步(bù)细化,高风险(xiǎn)的原料需要注意(yì)微生物危(wēi)害。
6. 化妆品原料以(yǐ)及其包材中可能含(hán)有的(de)杂质(zhì)需(xū)要进行风险(xiǎn)评估并证明其技术上是不可避免的(如GMP条件下也无法避免)。
7. 化妆品所使用的原料需要提供详细的毒理档(dàng)案(Toxicological Profile of Substance,TPS),每一个(gè)原料(liào)需要提供其毒理学信息,包括急性毒性、刺激性、过敏性等(děng)共12项毒理学端点。
8. 化妆品原材料和成品的生产商都需要达到GMP(ISO 22716)标准。 由于原料中的(de)杂质具有(yǒu)潜在的可以影响物(wù)质毒(dú)性的风险因素,因此在评估杂质的安全性时可以引入毒理学关注阈值(TTC)作为有效的评估手段。
9. 若出现不良反应,则需在报告中(zhōng)评估其发生的可能性和因果关系,出现(xiàn)严重的不良反应需(xū)上报欧盟(méng)成员国有关主(zhǔ)管部门,并在(zài)CPSR报告中以附(fù)件形式存在并描述处理和解决方法。
10. 在评估报(bào)告结论中必须提到新的化妆品法(fǎ)规Regulation(EC)1223/2009,并且明确(què)指出(chū)产品是否符(fú)合新的化妆品法规。
11. 关于产(chǎn)品标签,警告用(yòng)语和使用说明(míng)在满足新(xīn)法规外还须参考相(xiàng)关(guān)文件,如 Commission Recommendation 2006/647/EC 及其它与标签相关的指导文件。为了直观地表(biǎo)达该内容,可以在CPSR中附上产品的图片。
12. 毒理(lǐ)风(fēng)险评估(gū)由定性评估变为定量评估。包括产品(pǐn)系统性的(de)风险评估,配方组合后的(de)兼容性(xìng),稳定性,微生(shēng)物,包装,标签以及使用等各个方面。产品所有(yǒu)的测试报告、技术文档和其它相关信息须经过毒理风险评估师评估,并特别注意(yì)三岁以下儿童使(shǐ)用的产品(pǐn),除了满足(zú)新(xīn)法规要求还需遵循欧盟消费(fèi)者(zhě)安全科学委员会(huì)(SCCS)指南(nán)。
13. 当法律要求(qiú)出现变(biàn)化或更(gèng)改时,产品的原(yuán)材料发(fā)生改变(如更换供应(yīng)商),使(shǐ)用条件(jiàn)发生改变,以及监测到在正常使用条件下不良反应发生率增(zēng)加时,毒理风险评估师须对产(chǎn)品进行重(chóng)新评估,确保化妆品安全报告(CPSR)保持同步更新并满足(zú)新法规要(yào)求。
14. 指南对于可以出具化妆品安全报告(CPSR)的安全评估师资质做了详细的定义(yì),非欧(ōu)盟成员国承认的药学,毒理学等相关专业人员不得从(cóng)事化妆品安全报告评估(gū)工作。并且(qiě)评估师的资(zī)质及相(xiàng)关(guān)学历证明需要附在评估(gū)报告后。
相关信息/ RELATED INFO
MORE
服务热线
微信(xìn)扫一(yī)扫


返(fǎn)回顶部